Determinar la incidencia del cambio inmunitario del porcentaje de linfocitos T CD4+ en pacientes VIH 1/2 positivos en el primer trimestre posvacunación antigripal (P-CIR) y secundariamente comparar las características demográficas y clínicas relacionadas con dicho cambio.
MétodosSe estudiaron 105 pacientes con VIH-sida de una cohorte retrospectiva hospitalaria entre 2001 y 2006. Se consideró P-CIR una disminución >3% del porcentaje de CD4+ prevacunal, y su asociación cruda y ajustada (sexo, edad, terapia antirretroviral, estabilidad clínica, carga viral prevacunal, CD4 total prevacunal) fue evaluada por regresión logística (odds ratio [OR] con intervalo de confianza del 95% [IC95%]).
ResultadosLa incidencia del P-CIR fue del 33,3%, y fue persistente en un 31,4% durante los siete meses posvacunación independientemente de una viremia alta prevacunal. Asimismo, las variables demográficas y clínicas estudiadas no se relacionaron con la presencia de P-CIR, con una OR cruda de 0,90 (0,17–4,8) y una OR ajustada de 1,09 (0,17–6,8).
ConclusionesLos datos encontrados reflejan que el cambio relevante del estado inmunitario no fue despreciable en la posvacunación, aunque mayoritariamente resultó transitorio.
To determine the incidence of immunologic change in the percentage of CD4+ T lymphocytes in HIV 1/2 positive patients in the first quarter after influenza vaccination (P-CIR) and to compare the demographic and clinical characteristics associated with this change.
MethodsWe studied 105 patients with HIV/AIDS in a retrospective hospital cohort between 2001–2006. P-CIR was considered as a decrease of >3% in the prevaccination CD4+ percentage. Crude and adjusted OR (sex, age, antiretroviral therapy, clinical stability, prevaccination viremia and prevaccination total CD4) were evaluated by logistic regression (95%CI).
ResultsThe incidence of P-CIR was 33.3%. P-CIR was persistent in 31.4% for 7 months after vaccination regardless of high prevaccination viremia. No association was found between demographic and clinical variables and P-CIR [crude OR: 0.90 (0.17–4.8); adjusted OR: 1.09 (0.17–6.8)].
ConclusionsThe results showed that the immunological change after vaccination was not inconsiderable. However, this change was mainly transient.
En el año 2006 se notificaron en España 1.605 nuevos casos de sida1,2. El impacto de la infección por el virus de la gripe3,4,5 en las personas seropositivas para el VIH supone una mayor morbilidad en cuanto a intensidad, prolongación del tiempo de enfermedad y complicaciones. Por ello, la vacuna antigripal está recomendada por diversos expertos, tanto nacionales (Grupo de Trabajo Español de Vacunación de Adultos6, respaldado por el Ministerio de Sanidad y Consumo Español) como internacionales (Advisory Committee on Immunization Practices7 [ACIP], con el aval de los Centers for Disease Control and Prevention [CDC]). Se recomienda la aplicación anual de la vacuna antigripal al inicio de la temporada de la gripe en todo paciente VIH positivo mayor de 6 meses de edad, como pilar preventivo de la enfermedad y sus complicaciones.
Por otro lado, la información con respecto al impacto inmunitario de la vacuna antigripal en los pacientes VIH positivos es limitada, aunque se cree que la respuesta inmunitaria (anticuerpos contra la gripe) depende esencialmente de la cantidad de linfocitos T CD48. En el metaanálisis de Atashili et al9 con 646 sujetos VIH positivos se encontró una menor incidencia de gripe en los sujetos vacunados en comparación con los no vacunados, con un rango de diferencia de riesgos desde −0,48 (intervalo de confianza del 95% [IC95%]: −0,63 a −0,34) hasta −0,15 (IC95%: −0,25 a 0,05); se halló que es necesario vacunar de tres a siete personas para prevenir un caso de gripe. El rango de la efectividad de la vacuna fue del 27% al 78%; el 27% se relacionaba con un recuento de CD4 <200celulas/mm3.
Asimismo, existen resultados no concluyentes con respecto a los posibles efectos de la vacuna antigripal sobre la cantidad de CD4 y la viremia, desde cambios transitorios (entre 4-6 semanas y hasta tres meses después de la vacunación) en uno o en ambos parámetros10,11,12,13,14,15,16,17,18,19,20 hasta la no evidencia de cambios significativos21,22,23,24,25. Estos estudios son muy heterogéneos en cuanto a diseño, tamaño muestral, seguimiento, grado de inmunodepresión basal, deterioro inmunitario y tratamiento antirretroviral, así como en los resultados. Esta diversidad supone dificultades para hacer inferencias de los resultados para la propia población. Todo ello tendría su importancia clínico-epidemiológica, ya que teóricamente la vacunación podría incrementar la viremia en algunos pacientes VIH positivos, con la posibilidad de inducir una mutación genómica11 viral con repercusión en el tratamiento antirretroviral, y por consiguiente en la progresión de la enfermedad.
Los objetivos de nuestro estudio fueron: a) determinar la incidencia del cambio inmunitario del porcentaje de linfocitos T CD4+ en los pacientes VIH positivos a los 90 días de la vacunación antigripal, y b) comparar las características demográficas y clínicas de los pacientes VIH positivos con cambio inmunitario tras recibir la vacuna antigripal con los que no mostraron ningún cambio.
MétodosDiseño del estudioSe estudió una cohorte retrospectiva de pacientes con VIH-sida.
Población del estudioMuestra de base hospitalaria del Hospital Universitario de Bellvitge, de Barcelona (España), constituida por adultos vacunados visitados en la unidad de VIH-sida del Servicio de Enfermedades Infecciosas, que fueron derivados al Servicio de Medicina Preventiva para ser vacunados según protocolo durante los periodos invernales entre 2001 y 2006.
Criterios de elegibilidadLos criterios de inclusión fueron: a) pacientes VIH 1/2 positivos, de 18 años de edad en adelante; b) vacunados con vacuna antigripal en el Servicio de Medicina Preventiva del Hospital Universitario de Bellvitge entre 2001 y 2006; c) con datos de laboratorio del recuento y porcentaje de linfocitos T CD4+ y de la viremia del VIH 1/2 prevacunal (como máximo de tres meses antes) y posvacunal (durante los tres meses posteriores a la inmunización). Los pacientes eran excluidos si no cumplían alguno de los criterios de inclusión.
Variables estudiadas y sus definicionesVariable resultadoCambio mínimo inmunitario en el porcentaje de linfocitos T CD4 en el primer trimestre posvacunación (P-CIR).
Para este estudio se consideraron los cambios mínimos relevantes26 según la guía de práctica clínica de los CDC, circunscritas al primer trimestre posvacunación: en cuanto al porcentaje de linfocitos T CD4+, una disminución de más del 3% del basal (P-CIR); cuantificación absoluta de CD4 con una disminución de más del 30% del valor basal (cambio en CD4 total); para la carga viral un incremento de tres veces el valor basal (cambio en la viremia). Se optó por el porcentaje de CD4 porque tiene menos variabilidad entre medidas y una correlación clínica mayor que la cuantificación de CD4, y por ello se utilizó como marcador de la depleción inmunitaria posvacunación.27,28
En los pacientes con P-CIR se analizó el cambio más próximo a la vacunación (dentro del primer trimestre posvacunación) y se consideró como transitorio si desaparecía durante los siete meses posvacunación.
Variables independientesRecuento de CD4 total prevacunal, viremia prevacunal, tratamiento antirretroviral, estabilidad clínica respecto al VIH, vacunación concomitante con otras vacunas, edad y sexo.
Para cuantificar la viremia se usó la técnica de reacción en cadena de la polimerasa (PCR) y el límite inferior de detección fue de 40copias/ml. Para el recuento y el porcentaje de linfocitos T CD4 se usó citometría de flujo.
El «período prevacunal» máximo comprendió los tres meses previos a la inmunización. Se consideró «vacunación concomitante» la coadministración de una o más vacunas en un plazo de ± 15 días: antihepatitis B, antihepatitis A, antineumocócica o antitetánica. El «estado clínico»29 consideraba estar asintomático o no respecto al VIH durante el período de seguimiento. La variable «estado inmunitario basal» categorizaba29 según el recuento de linfocitos T CD4: menos de 200pormm3 (inmunodepresión grave), entre 200 y 499pormm3 (moderada) y 500 o más por mm3 (leve).
El tratamiento antirretroviral se entendió como el uso de inhibidores de la transcriptasa reversa análogos de nucleósidos y nucleótidos, de inhibidores de la transcriptasa reversa no nucleósidos, de inhibidores de las proteasas o de inhibidores de la fusión26. El tratamiento antirretroviral se estudió (previo a la vacunación y hasta tres meses después de ésta) de manera dicotómica (ausencia o presencia) y según grupos terapéuticos.
Fuentes de informaciónMediante revisión sistemática del registro vacunal del Servicio de Medicina Preventiva, la información se obtuvo de las historias clínicas y de los informes electrónicos de hematología, inmunología y microbiología del Hospital Universitario de Bellvitge.
Tanto los análisis de laboratorio como el tratamiento antirretroviral se realizaron según el criterio clínico del médico responsable de la Unidad de VIH-sida del Hospital Universitario de Bellvitge, de manera protocolizada según la práctica clínica habitual cada tres a cuatro meses.
IntervenciónLa vacuna antigripal usada en los períodos invernales entre 2001 y 2006 fue la polivalente de virus fraccionados según las cepas análogas recomendadas por la OMS para cada temporada invernal: en 2001–2002, A/Panama/2007/99 (H3N2), A/New Caledonia/20/99 (H1N1) y B/Sichuan/379/99; en 2002–2003, A/New Caledonia/20/99 (H1N1), A/Panama/2007/99 (H3N2) y B/Hong Kong/330/2001; en 2003–2004, A/New Caledonia/20/99 (H1N1), A/Panama/2007/99 (H3N2) y B/HongKong/330/2001; en 2004–2005, A/New Caledonia/20/99 (H1N1), A/Fujian/411/2002 (H3N2) y B/Shanghai/361/2002; en 2005–2006, A/New Caledonia/20/99 (H1N1), A/California/7/2004 (H3N2) y B/Shanghai/361/2002; y en 2006–2007, A/New Caledonia/20/1999 (H1N1), A/Wisconsin/67/2005 (H3N2) y B/Malaysia/2506/2004.
Los pacientes registrados podían ser vacunados contra la gripe en más de una ocasión, considerando el período de estudio (seis años) y la política sanitaria nacional de vacunación en grupos de riesgo. Por ello se analizaron todos los casos encontrados de forma semejante, tanto para el análisis estadístico como para el epidemiológico.
Estimación del tamaño muestralNo fue posible hacer el cálculo debido a la falta de datos en la literatura en relación con la variable principal de cambio inmunitario, y por tanto se eligió una muestra por conveniencia, una de las más grandes respecto a estudios previos, y compatible con el servicio donde se desarrolló el estudio.
Análisis estadísticoSe realizó un análisis descriptivo de las variables cualitativas según las frecuencias y los porcentajes; y de las cuantitativas según las medidas de tendencia central y la dispersión. Las variables cuantitativas, dependiendo de su normalidad (estudiada según el test de Kolmogorov-Smirnov, p>0,05), se definieron según la media y la desviación estándar, y en caso contrario según la mediana y el rango intercuartílico (RIC).
Se estudio la asociación de P-CIR con las variables cualitativas según el test ji-cuadrado o el de Fisher (cuando las frecuencias esperadas son inferiores a 5 en un 20% o más de la muestra), y con las cuantitativas según el test t de Student apareado (CD4 porcentaje) al cumplir los criterios de normalidad (Kolmogorov-Smirnov, p>0,05), y por defecto con el test no paramétrico U de Mann Whitney (edad, viremia, CD4 total).
La hipótesis inicial del modelo consideró como factor predictor principal el recuento de CD4 total prevacunal, y como covariables la viremia prevacunal, el tratamiento antirretroviral, la estabilidad clínica, el sexo y la edad (potenciales confusores o modificadores).
La asociación entre las variables independientes y P-CIR fue evaluada por regresión logística y se obtuvieron las odds ratio (OR) con sus intervalos de confianza del 95% (IC95%). Se valoró la magnitud de la asociación controlada por las covariables y la estimación cruda (sin ajustar por factores confusores).
La precisión predictiva y la calibración del modelo se establecieron con el test de la bondad de ajuste según Hosmer-Lemeshow y el área bajo la curva operacional del receptor (ROC). Se consideró el IC95% y el valor p (estadísticamente significativo si p<0,05). Se utilizó el paquete estadístico SPSS 15.0 (Chicago, Illinois).
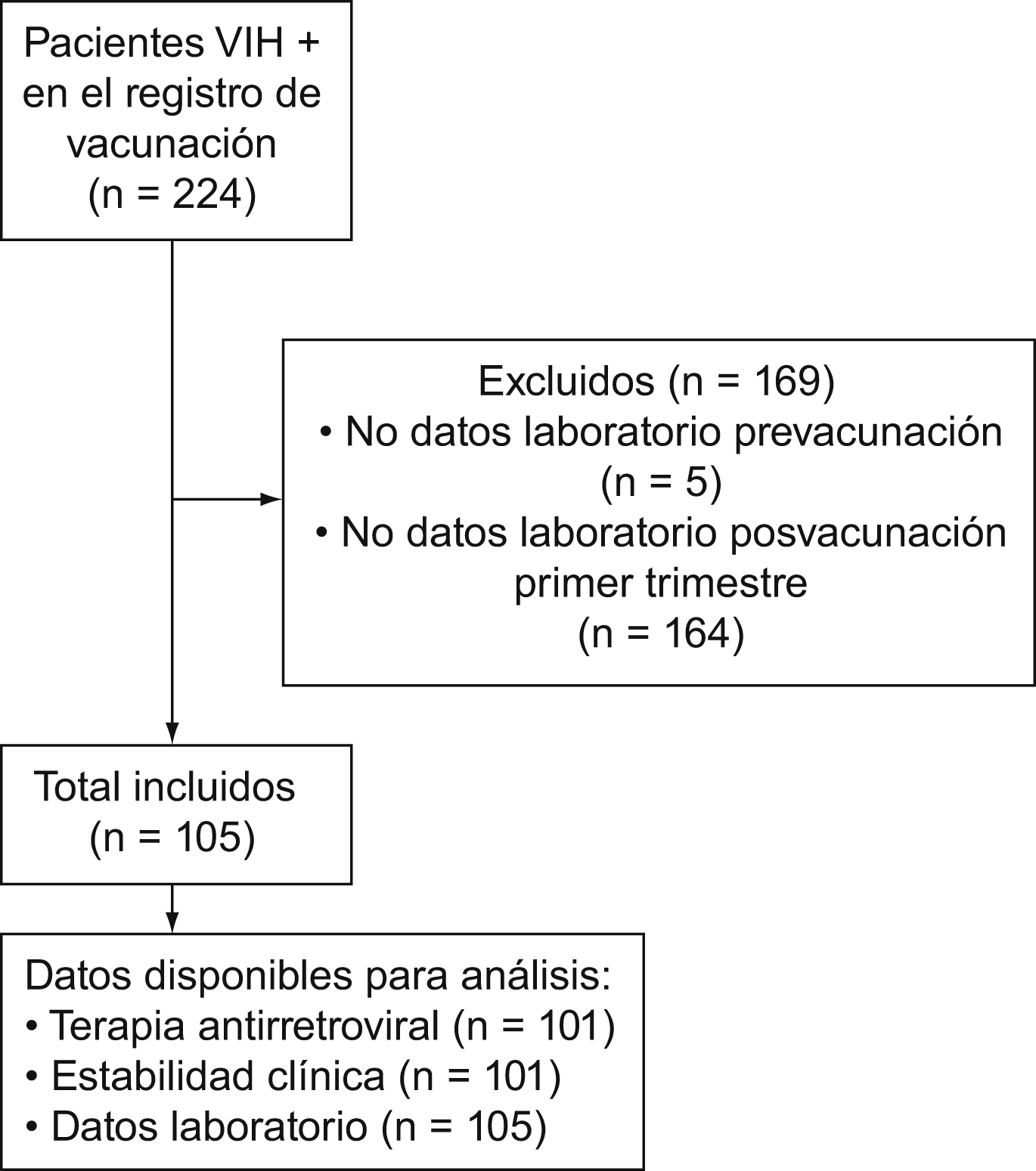
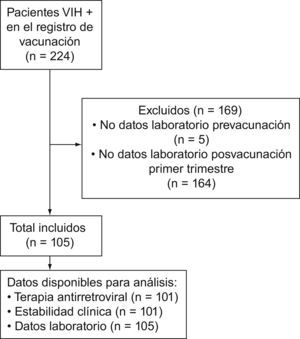
ResultadosDe los 274 pacientes VIH positivos que recibieron la vacuna antigripal, 105 cumplieron los criterios de inclusión (figura 1). El 18,1% (19/105) de los pacientes aportó más de un caso, pero se analizaron los 105 casos sin distinciones.
Figura 1. Diagrama de elección de la muestra del estudio.
Las características basales de la población estudiada se muestran en la tabla 1, donde puede verse que la mediana de edad fue de 40 años, predominaban los hombres (77%), el estado de inmunodepresión leve a moderada (96,1%), sin vacunación concomitante (68,6%), y el tratamiento antirretroviral (80%) con 245 días de mediana (RIC: 205–280). El 96,2% estaban clínicamente estables y asintomáticos respecto al VIH durante todo el seguimiento posvacunal.
Tabla 1. Características basales de los pacientes VIH positivos
| Cambio relevante del porcentaje de linfocitos T CD4+ en el primer trimestre posvacunación | ||||
| Variable | Total sujetos (n=105) | No (n=70) | Sí (n=35) | p a |
| Edad, mediana (RIC b ), años | 40 (35–45) | 40 (35–44) | 41 (34–48) | 0,678 |
| Sexo, n (%) | ||||
| Mujer | 24 (22,9) | 15 (21,4) | 9 (25,7) | 0,622 |
| Hombre | 81 (77,1) | 55 (78,6) | 26 (74,3) | |
| Estado inmunitario basal, n (%) | ||||
| <200 células/mm3 | 4 (3,8) | 3 (4,3) | 1 (2,9) | 0,803 |
| 200–499 células/mm3 | 60 (57,1) | 40 (57,1) | 20 (57,1) | |
| ≥500 células/mm3 | 41 (39,0) | 27 (38,6) | 14 (40,0) | |
| Vacunación concomitante c , n (%) | ||||
| No | 72 (68,6) | 49 (70,0) | 23 (65,7) | 0,656 |
| Sí | 33 (31,4) | 21 (30,0) | 12 (34,3) | |
| Terapia antirretroviral prevacunal, n (%) | ||||
| No | 17 (16,2) | 12 (17,1) | 5 (14,3) | 0,684 |
| Sí | 84 (80,0) | 55 (78,6) | 29 (82,9) | |
| Información pérdida | 4 (3,8) | 3 (4,3) | 1 (2,9) | |
| Estabilidad clínica, n (%) | ||||
| No | 0 (0,0) | 0 (0,0) | 0 (0,0) | 0,712 |
| Sí | 101 (96,2) | 67 (95,7) | 34 (97,1) | |
| Información pérdida | 4 (3,8) | 3 (4,3) | 1 (2,9) | |
| Carga viral, mediana (RIC), copias/ml | 80 (80–80) | 80 (80–80) | 80 (80–146) | 0,804 |
| Recuento CD4, mediana (RIC), células/mm3 | 437 (336–592) | 420 (313–570) | 445 (345–601) | 0,559 |
| Porcentaje T CD4, media (DE d ) | 23,70 (8,65) | 23,46 (8,94) | 24,20 (8,13) | 0,680 |
a Contraste de hipótesis entre «cambio sí/no», p>0,05 indica diferencia estadísticamente no significativa.
b Rango intercuartílico, indica el percentil 25 al 75.
c Vacunación paralela contra el tétanos, el neumococo, la hepatitis A o la hepatitis B.
d Desviación estándar.
Entre los dos grupos que constituyen el P-CIR (sí/no cambio) no hubo diferencias estadísticamente significativas (p>0,05) con respecto a las características basales (tabla 1) de sexo, edad, estado inmunitario, tratamiento antirretroviral, vacunación concomitante, estabilidad clínica, recuento y porcentaje de linfocitos T CD4, y viremia prevacunal.
También se categorizó la variable «recuento de CD4 prevacunal» en dos grupos: <350 (sí cambio 9/34) y ≥350 (sí cambio 26/71), teniendo en cuenta que es el punto de corte para proponer el inicio del tratamiento antirretroviral a los pacientes VIH asintomáticos26,30; no se encontraron diferencias significativas entre ellos (p=0,30).
Tampoco hubo diferencias estadísticamente significativas (p>0,05) con las variables estudiadas posvacunación (tabla 2): tratamiento antirretroviral, estabilidad clínica, cuantificación de linfocitos T CD4 y viremia.
Tabla 2. Variables en el primer trimestre posvacunación
| Cambio relevante del porcentaje de linfocitos T CD4+ en el primer trimestre posvacunación | ||||
| Variable | Total sujetos (n=105) | No (n=70) | Sí (n=35) | p a |
| Carga viral, mediana (RIC b ), copias/ml | 80 (80–80) | 80 (80–80) | 80 (80–370) | 0,668 |
| Cuantificación CD4, mediana (RIC), células/mm3 | 437 (348–610) | 474 (360–634) | 391 (313–529) | 0,075 |
| Porcentaje T CD4, media (DE c ) | 24,21 (9,19) | 25,91 (9,31) | 20,80 (8,02) | 0,007 |
| Terapia antirretroviral, n (%) | ||||
| No | 13 (12,4) | 8 (11,4) | 5 (14,3) | 0,807 |
| Grupo 1 (IP+INTI) d | 19 (18,1) | 14 (20,0) | 5 (14,3) | |
| Grupo 2 (IP+INTI+INNTI) e | 6 (5,7) | 5 (7,1) | 1 (2,9) | |
| Grupo 3 (INTI) f | 15 (14,3) | 10 (14,3) | 5 (14,3) | |
| Grupo 4 (INTI+INNTI) g | 44 (41,9) | 28 (40,0) | 16 (45,7) | |
| Información perdida | 8 (7,6) | 5 (7,1) | 3 (8,6) | |
| Terapia antirretroviral, n (%) | ||||
| Sí h | 84 (80,0) | 57 (81,4) | 27 (77,1) | 0,753 |
| No | 13 (12,4) | 8 (11,4) | 5 (14,3) | |
| Información perdida | 8 (7,6) | 5 (7,1) | 3 (8,6) | |
| Cambio de manejo terapéutico, n (%) | ||||
| No | 62 (59,0) | 41 (58,6) | 21 (60,0) | 0,813 |
| Sí | 38 (36,2) | 26 (37,1) | 12 (34,3) | |
| Información pérdida i | 5 (4,8) | 3 (4,3) | 2 (5,8) | |
a Contraste de hipótesis entre «cambio sí/no», p>0,05 indica diferencia estadísticamente no significativa.
b Rango intercuartílico indica el percentil 25 al 75.
c Desviación estándar.
d Grupo 1: combinación de inhibidores de la proteasa e inhibidores nucleósidos de la transcriptasa inversa.
e Grupo 2: combinación de inhibidores de la proteasa, inhibidores nucleósidos y no nucleósidos de la transcriptasa inversa.
f Grupo 3: inhibidores nucleósidos de la transcriptasa inversa.
g Grupo 4: combinación de inhibidores nucleósidos y no nucleósidos de la transcriptasa inversa.
h Agrupado: grupos del 1 al 4.
i Se incluyen tres pacientes que abandonaron el tratamiento antirretroviral en el período posvacunal.
La hipótesis inicial del modelo consideraba como predictor principal el recuento de CD4 total prevacunal, y como covariables la viremia, el tratamiento antirretroviral, el sexo y la edad (tabla 3). La estabilidad clínica no se incluyó porque todos los pacientes se mantuvieron asintomáticos con respecto al VIH durante el período de estudio. Las variables sexo y edad no se halló que fueran estadísticamente variables confusoras ni interactoras dentro del modelo, pero se introdujeron por su valor clínico. La OR cruda del P-CIR fue 0,90 (0,17–4,8) al incrementar en una unidad el CD4 total prevacunal, y la OR ajustada fue 1,12 (0,18–6,9), ambas estadísticamente no significativas. Se realizó la prueba de bondad de ajuste (p=0,277) y el área bajo la curva ROC, y se obtuvo un 55,8% con un IC95% de 43,6 a 68,1%.
Tabla 3. Asociación entre cambio inmunitario relevante del porcentaje de CD4 en el primer trimestre posvacunación y las variables independientes. Regresión logística univariado
| Cambio relevante del porcentaje de linfocitos T CD4+ en el primer trimestre posvacunación (sí/no) | ||
| Univariado | ||
| Variables | OR cruda (IC95%) | p |
| CD4 total prevacunal | 0,90 (0,17–4,8) | 0,9 |
| Edad | 1,01 (0,97–1,05) | 0,83 |
| Sexo | ||
| Mujer (referencia) | ||
| Hombre | 0,79 (0,31–2,04) | 0,62 |
| Tratamiento antirretroviral prevacunal | ||
| No (referencia) | ||
| Sí | 1,27 (0,41–3,94) | 0,69 |
| Tratamiento antirretroviral posvacunal | ||
| No tratamiento antirretroviral (referencia) | ||
| Grupo 1 a | 0,57 (0,13–2,60) | 0,47 |
| Grupo 2 b | 0,32 (0,03–3,60) | 0,36 |
| Grupo 3 c | 0,80 (0,17–3,77) | 0,78 |
| Grupo 4 d | 0,91 (0,26–3,27) | 0,89 |
| Tratamiento antirretroviral posvacunal | ||
| No (referencia) | ||
| Sí e | 0,76 (0,23–2,54) | 0,65 |
| Carga viral prevacunal | 1,00 (1,00–1,00) | 0,32 |
| Cambio de manejo terapéutico | ||
| No (referencia) | ||
| Sí | 0,90 (0,38–2,14) | 0,81 |
IC: intervalo de confianza; OR: odds ratio.
a Combinación de tratamiento antirretroviral: inhibidores de la proteasa, inhibidores nucleósidos de la transcriptasa inversa.
b Combinación: inhibidores de la proteasa, inhibidores nucleósidos y no nucleósidos de la transcriptasa inversa.
c Inhibidores nucleósidos de la transcriptasa inversa.
d Combinación de inhibidores nucleósidos y no nucleósidos de la transcriptasa inversa.
e Agrupado: grupos del 1 al 4.
Se encontró P-CIR en un 33,3% (35/105) de los pacientes. De ellos, fue transitorio en el 60,0% (21/35), persistente en el 31,4% (11/35), y no hubo información del 8,6% (3/35).
De los 35 casos con P-CIR, en el 7,2% coincidió con un cambio en los CD4 totales o en la viremia.
Tratamiento antirretroviralDos pacientes (2/84) que antes de recibir la vacuna estaban en tratamiento antirretroviral cambiaron de familia antirretroviral en el primer trimestre posvacunación. También hubo un 41,7% (35/84) de cambios en fármacos antirretrovirales, de los cuales un 40,0% (14/35) fue por el inicio de un ensayo clínico, un 25,7% (9/35) por efectos adversos, un 20,0% (7/35) por simplificación del tratamiento, un 8,6% (3/35) tras una prueba de resistencia, y un 5,7% (2/35) por terapia conjunta contra el virus de la hepatitis B.
De los 17 pacientes que antes de la vacunación antigripal no estaban en tratamiento antirretroviral (considerando también los que lo suspendieron, el tiempo mínimo de suspensión encontrado fue de 115 días antes de la vacunación), un 35,3% (6/17) iniciaron el tratamiento antirretroviral en el primer trimestre posvacunación. Se observó un 29,4% (5/17) con P-CIR, en el 40% de los casos transitorio. Un paciente presentó un cambio relevante de CD4 total transitorio y no hubo cambio relevante de la viremia.
Algunos estudios asocian la combinación de tenofovir y didanosina con una disminución paradójica de linfocitos CD4. En este estudio, antes de recibir la vacuna hubo ocho pacientes y en el período posvacunal fueron cinco. No hubo diferencia estadísticamente significativa con respecto a la presencia de P-CIR (prevacunal p=0,82; posvacunal p=0,69).
Al evaluar el P-CIR y el «cambio de manejo terapéutico» (aquellos que antes de la vacunación no recibían tratamiento antirretroviral y luego lo iniciaron, o aquellos que en el período posvacunal cambiaron de esquema de tratamiento antirretroviral o lo suspendieron) no se encontraron diferencias estadísticamente significativas (prueba de ji-cuadrado, p=0,813).
Se realizó nuevamente el análisis multivariado (tabla 4) incluyendo la variable «cambio de manejo terapéutico» a la hipótesis original (dada su posible relevancia clínica), y se halló una OR ajustada del P-CIR de 1,09 (0,17–6,78) al incrementar en una unidad el CD4 total prevacunal, resultando estadísticamente no significativo. Se realizaron la prueba de bondad de ajuste (p=0,741) y el área bajo la curva ROC, y se obtuvo un 58,1% y un IC95% de 46,1 a 70,1%. Es decir, las variables seleccionadas no predecían adecuadamente la presencia o no de P-CIR.
Tabla 4. Asociación entre recuento de linfocitos T CD4+ prevacunal y cambio inmunitario relevante del porcentaje de CD4+ en el primer trimestre posvacunación
| Cambio relevante del porcentaje de linfocitos T CD4+ en el primer trimestre posvacunación (sí/no) | ||||||||
| Univariado a | Ajustado b por sexo y edad | Ajustado c además por | Multivariado ajustado d | |||||
| OR (IC95%) | p | OR (IC 95%) | p | OR (IC95%) | p | OR (IC95%) | p | |
| CD4 total prevacunal | 0,90 (0,17–4,8) | 0,90 | 1,0 (0,18–5,70) | 0,99 | Tratamiento antirretroviral prevacunal: 0,90 (0,16–5,2) | 0,91 | 1,09 (0,17–6,8) | 0,93 |
| Tratamiento antirretroviral posvacunal: 1,16 (0,19–7,07) | 0,88 | |||||||
| Carga viral prevacunal: 1,09 (0,19–6,20) | 0,92 | |||||||
| Cambio de manejo terapéutico: 0,93 (0,16–5,44) | 0,94 | |||||||
IC: intervalo de confianza; OR: odds ratio.
a CD4 total prevacunal: OR cruda (con IC95%) y valor p.
b CD4 total prevacunal ajustado por edad y sexo: OR ajustada (con IC95%) y valor p.
c CD4 total prevacunal ajustado por edad, sexo y además por alguno de los siguientes: tratamiento antirretroviral prevacunal o posvacunal o carga viral prevacunal o cambio de manejo terapéutico.
d CD4 total prevacunal ajustado por todas las variables independientes: sexo, edad, carga viral prevacunal, tratamiento antirretroviral prevacunal, tratamiento antirretroviral posvacunal y cambio de manejo terapéutico.
En este estudio, la incidencia del cambio inmunitario relevante26 en el porcentaje de CD4 fue del 33,3% (persistente en el 31,4%), sin asociarse con viremia alta prevacunal. Asimismo, las variables demográficas y clínicas estudiadas no se relacionaron con la aparición de P-CIR.
En contraste, la probabilidad de observar cambios relevantes26 parece variar según el parámetro que se analice, cuantificación de CD4 y viremia, en un 4,8%.
Se optó por el porcentaje de CD4 porque es más estable, con una mayor fidelidad y correlación clínica que la cuantificación de CD417, y por ello se utilizó como marcador de la depleción inmunitaria posvacunación. Además, según la literatura revisada, los pacientes en tratamiento antirretroviral presentan una viremia que disminuye significativamente, hasta hacerse indetectable clínicamente, aunque los linfocitos T CD4+ infectados pueden permanecer como reservorio estable intrínseco latente de viremia, imposibilitando la erradicación del virus31.
Los estudios previos10,12,14,15,16,17,18,19,22 con seguimientos a corto plazo no han encontrado evidencias de deterioro clínico debido a cambios en el recuento de CD4 o en la viremia inducidos por la inmunización antigripal. En estos estudios, el tamaño de la muestra era pequeño (n<50), el número de pacientes con inmunodepresión grave (n<10) bastante escaso (incluyendo el presente estudio) y el tiempo de seguimiento corto (< 20 semanas).
Nuestro estudio focalizó sus esfuerzos al considerar un cambio inmunitario relevante, con un seguimiento más largo (siete meses) y un mayor tamaño muestral (n=105), lo cual dificulta su comparación con estudios precedentes.
En estudios previos,10,12,14,15,16,17,18,19,22 el cambio en el RNA viral iba del 18,8%22 al 83,0%,14 y en la cuantificación de CD4 del 45%15 al 60%,12 en contraste con la incidencia de cambio relevante (CD4, RNA) encontrada en nuestro estudio, que fue notablemente inferior (4,8%), probablemente porque hablamos de cambios relevantes en vez de sólo cambios cuantitativos. Por otro lado, se desconoce si el cambio percibido fue debido a la vacunación o a una progresión de la enfermedad, ya que no hubo posibilidad de comparación con una cohorte de pacientes VIH positivos no inmunizada, aunque en este estudio el 96,2% de los pacientes se mantuvieron asintomáticos respecto al VIH durante todo el período de seguimiento. El porcentaje no despreciable de pacientes que cambiaron su esquema de tratamiento antirretroviral después de la vacunación (41,7%) también podría enmascarar los posibles efectos de la vacunación o de la enfermedad en cuanto a la replicación viral, aunque sólo dos de 84 pacientes cambiaron de familia antirretroviral y en general hay una importante y durable supresión de la viremia, con restauración o preservación de la función inmunitaria.
Nuestros resultados han podido verse afectados por un sesgo de selección, pues los participantes son de base hospitalaria, dado que acudían al Servicio de Medicina Preventiva del Hospital Universitario de Bellvitge para ser vacunados. Debido a la naturaleza del diseño retrospectivo se estudió el 40% de los pacientes potencialmente elegibles por disponer de datos de laboratorio antes y después de la vacunación, lo cual podría suponer una mayor representación de casos más complejos, con mayor gravedad de la infección o más adherencia al tratamiento antirretroviral.
Otra posible limitación ha sido tener un tamaño insuficiente de muestra en la categoría de inmunodepresión grave (aunque éste no era nuestro objetivo principal), ya que con el tratamiento antirretroviral actual es inusual tener pacientes en estas condiciones de inmunodepresión grave. Precisamente, la causa principal de la inmunodepresión grave es el fallo terapéutico. Existe controversia y necesidad de mayor investigación (debido también a la baja efectividad de la vacuna antigripal) tanto para los inmunodeprimidos graves (CD4<200) como para los adultos de edad avanzada7,32.
Es necesario añadir que el protocolo de actuación entre el Servicio de Medicina Preventiva y la Unidad de VIH-sida tiene como objeto promover las vacunaciones recomendadas en este grupo de riesgo aprovechando la estrecha colaboración y la gran accesibilidad entre ellos. El tener pocos pacientes VIH positivos con menos de 200 CD4 podría obedecer a la valoración del riesgo-beneficio (a priori) que realizan los médicos tratantes, por lo cual la muestra podría reflejar lo que sucede en la práctica clínica cotidiana.
Debido a la política sanitaria de implementación de la vacuna antigripal nos fue imposible tener un grupo control (sin ningún antecedente de vacunación antigripal), pues no podría asegurarse la no vacunación en otros centros. El diseño del estudio (observacional) no interactuó éticamente con la indicación de la vacuna en este grupo de riesgo.
Otras limitaciones del estudio fueron que no se pudo recopilar sistemáticamente los datos sobre los antecedentes patológicos, ni sobre la adherencia al tratamiento antirretroviral como determinante clave en el grado y la duración de la supresión virológica, por no estar recogidos de manera sistemática en la historia clínica. Existen importantes dificultades para definir la adherencia26, por la discrepancia entre médico y paciente y por su baja sensibilidad. Una aproximación, actualmente discutida, es una combinación de fuentes: autorreporte de dosis recientes (≤3 días) y registrada desde la última visita. Esto podría considerarse en estudios futuros.
Finalmente, los datos encontrados en el estudio reflejan que el cambio relevante del estado inmunitario no fue despreciable después del primer trimestre posvacunación, aunque mayoritariamente resultó transitorio. Este grupo de pacientes es considerado de riesgo y en ellos recomendamos la vacunación antigripal, aunque creemos que son necesarios más estudios para la categoría de inmunodepresión grave, que valoren su bioseguridad y efectividad.
Agradecimientos
A las enfermeras del Servicio de Medicina Preventiva del Hospital Universitario de Bellvitge por mantener el registro actualizado de vacunados del servicio. A la Unidad de VIH-sida del Servicio de Enfermedades Infecciosas del Hospital Universitario de Bellvitge.
Financiación
Este trabajo no fue financiado.
Conflicto de intereses
Los autores no tienen relación comercial ni de otro tipo que pudiera suponer algún conflicto de intereses.
Recibido 7 Mayo 2008
Aceptado 3 Noviembre 2008
Autor para correspondencia. cmasuet@csub.scs.es