El programa de vacunación contra la COVID-19 involucra múltiples procesos dinámicos que cambian con la evidencia científica disponible. Se sabe que la efectividad de las diferentes vacunas varía entre un 50% y un 95%; también se sabe que existe una relación entre los títulos de anticuerpos neutralizantes y la protección inmunitaria frente a la infección sintomática producida por el SARS-CoV-21. Sin embargo, se desconoce la duración de esta inmunidad protectora que brindan las vacunas frente a las diferentes variantes del SARCS-CoV22,3.
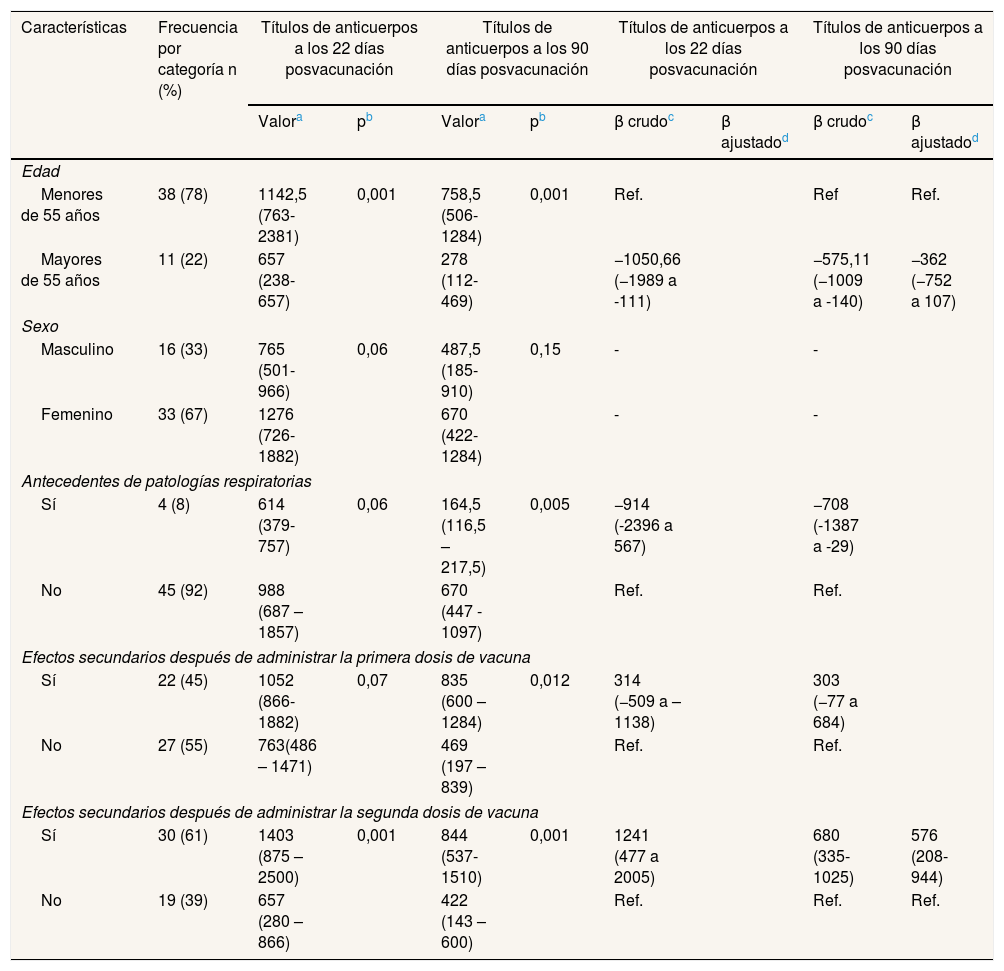
Como parte de un estudio longitudinal aprobado por el Comité de Investigación del Departamento de Salud de Dénia, se han cuantificado los títulos de anticuerpos contra el SARS-CoV-2 del dominio de unión antirreceptor (RBD) de la proteína Spike (S) en 49 miembros del personal del Centro de Salud de Jávea (de los 56 que lo componen) que cumplían los criterios de inclusión: no tener una prueba PCR positiva para SARS-CoV-2 documentada previamente y no tener registro de haber estado en aislamiento por ser contacto estrecho. Para la cuantificación de los anticuerpos se utilizó la prueba Elecsys Anti-SARS-CoV2, de Roche4. El análisis de anticuerpos se realizó en dos momentos tras completar la pauta completa de la vacuna BNT162b2: M1 a los 22 días y M2 a los 90 días. Los/las participantes firmaron un consentimiento informado. En los primeros resultados (tabla 1) se observó que la mediana del título de anticuerpos era mayor en los menores de 55 años (en el M1 un 42,4% y en el M2 un 63,3%) que en los mayores de esta edad; la disminución de la mediana del título de anticuerpos en el M2 fue de un 33,6% en los menores de 55 años y de un 57,6% en los mayores. Un 61% de los/las participantes manifestaron haber tenido efectos secundarios sistémicos o locales5 después de recibir la segunda dosis de la vacuna; en estos participantes se observó una mediana mayor del título de anticuerpos estadísticamente significativa respecto a los que manifestaron no tener molestias.
Características demográficas y clínicas de los/las participantes del estudio, respecto al título de anticuerpos después las dos dosis de vacuna BNT162b2
| Características | Frecuencia por categoría n (%) | Títulos de anticuerpos a los 22 días posvacunación | Títulos de anticuerpos a los 90 días posvacunación | Títulos de anticuerpos a los 22 días posvacunación | Títulos de anticuerpos a los 90 días posvacunación | ||||
|---|---|---|---|---|---|---|---|---|---|
| Valora | pb | Valora | pb | β crudoc | β ajustadod | β crudoc | β ajustadod | ||
| Edad | |||||||||
| Menores de 55 años | 38 (78) | 1142,5 (763-2381) | 0,001 | 758,5 (506-1284) | 0,001 | Ref. | Ref | Ref. | |
| Mayores de 55 años | 11 (22) | 657 (238-657) | 278 (112-469) | −1050,66 (−1989 a -111) | −575,11 (−1009 a -140) | −362 (−752 a 107) | |||
| Sexo | |||||||||
| Masculino | 16 (33) | 765 (501-966) | 0,06 | 487,5 (185-910) | 0,15 | - | - | ||
| Femenino | 33 (67) | 1276 (726-1882) | 670 (422-1284) | - | - | ||||
| Antecedentes de patologías respiratorias | |||||||||
| Sí | 4 (8) | 614 (379-757) | 0,06 | 164,5 (116,5 – 217,5) | 0,005 | −914 (-2396 a 567) | −708 (-1387 a -29) | ||
| No | 45 (92) | 988 (687 – 1857) | 670 (447 - 1097) | Ref. | Ref. | ||||
| Efectos secundarios después de administrar la primera dosis de vacuna | |||||||||
| Sí | 22 (45) | 1052 (866- 1882) | 0,07 | 835 (600 – 1284) | 0,012 | 314 (−509 a – 1138) | 303 (−77 a 684) | ||
| No | 27 (55) | 763(486 – 1471) | 469 (197 – 839) | Ref. | Ref. | ||||
| Efectos secundarios después de administrar la segunda dosis de vacuna | |||||||||
| Sí | 30 (61) | 1403 (875 – 2500) | 0,001 | 844 (537-1510) | 0,001 | 1241 (477 a 2005) | 680 (335- 1025) | 576 (208-944) | |
| No | 19 (39) | 657 (280 – 866) | 422 (143 – 600) | Ref. | Ref. | Ref. | |||
Si bien solo se cuantificó parte de la inmunidad humoral, se evidenció que después de la vacunación todos los participantes tenían títulos de anticuerpos detectables; que los títulos de anticuerpos disminuyeron con el tiempo; que la mayor reactogenicidad ante la segunda dosis de la vacuna se asoció con una mayor inmunogenicidad; y que hasta el M2 ningún participante había enfermado de COVID-19.
Los datos recogidos indican la importancia de continuar investigando el tiempo de protección que brindan las vacunas, considerando la edad como una variable que determine las futuras pautas de vacunación.
Contribuciones de autoríaAmbas personas firmantes han contribuido igualmente en la concepción y el diseño del trabajo, la recogida de datos y su análisis, la interpretación de los resultados, la redacción y la revisión de la carta, y han aprobado la versión final para su publicación.
FinanciaciónNinguna.
Conflictos de interesesNinguno.