Describir la estrategia del Programa de Cribado de Cáncer Colorrectal en el País Vasco y los principales resultados de participación en la primera ronda (2009-2011).
MétodoEstudio retrospectivo de las invitaciones realizadas en 2009-2011 y comparación de las tasas de participación y positividad de la prueba de sangre oculta en heces por sexo y grupos de edad.
ResultadosSe obtuvieron 235.371 invitaciones válidas (personas correctamente localizadas), con una participación media del 64,3% (intervalo de confianza del 95% [IC95%]: 64,1-64,5) y con diferencias significativas (p<0,001) entre mujeres (67,1%; IC95%: 66,9-67,4) y hombres (61,4%; IC95%: 61,1-61,7). El porcentaje de positivos fue superior (p<0,001) en los hombres (9,1%; IC95%: 8,9-9,2) que en las mujeres (4,8%; IC95%: 4,7-4,9).
ConclusionesLas tasas de participación en el programa se consideraron adecuadas en comparación con los estudios revisados. Estas tasas podrían estar relacionadas con la estrategia de invitación y con factores culturales y sociales.
To describe the procedures of the colorectal cancer screening program in the Basque Country (Spain), and the main results of the first rounds in 2009-2011.
MethodWe carried out a retrospective study of invitations to attend screening between 2009 and 2011. Participation rates and the number of positive results of the fecal occult blood test (FOBT) were analyzed by sex and age group.
ResultsThere were 235.371 valid invitations (sent to the correct addresses), with an average participation rate of 64.3% (95%CI: 64.1-64.5%). Significant differences were found (p<0,001) between women (67.1%; 95%CI: 66.9-67.4) and men (61.4%; 95%CI: 61.1-61.7). The rate of positive FOBT results was higher (p<0,001) among men (9.1%; 95%CI: 8.9-9.2) than among women (4.8%; 95%CI: 4.7-4.9).
ConclusionsParticipation rates were adequate compared with those in the reviewed literature. These rates were probably affected by the invitation strategy and by cultural and social factors.
El cáncer colorrectal es el tercer tumor más frecuente en el mundo y el cuarto en mortalidad,1 y el más frecuente en España en ambos sexos, con un porcentaje de cambio anual del 2,5% (2,8% en los hombres y 2,17% en las mujeres, entre los años 1975 y 2004).2 El cribado poblacional se relaciona con la disminución de la morbilidad y la mortalidad,3 y desde 2003 es una recomendación europea su realización mediante la prueba de sangre oculta en heces (SOH).4 El Sistema Nacional de Salud asumió esta recomendación en su estrategia contra el cáncer,5 que se actualizó en 2009 proponiendo una cobertura poblacional del 50% para 2015.6 La Alianza para la Prevención del Cáncer de Colon actúa potenciando esta estrategia como foro profesional y ciudadano.7
El uso, en el cribado, de pruebas de SOH inmunoquímicas cuantitativas ha registrado mayores tasas de participación y de detección de lesiones que las químicas,8 por lo que son las recomendadas en las guías europeas.9 Asimismo, no se han hallado diferencias significativas en la detección de cáncer invasivo entre esta prueba y el otro método más utilizado en la primera ronda de cribado (colonoscopia directa).10
La tasa de participación se ha relacionado con el coste-efectividad11 de los programas de cribado, y se han llevado a cabo estrategias para su mejora, entre las que cabe destacar la implicación de los médicos de atención primaria y el envío de pruebas por correo. El nivel socioeconómico, el sexo y la edad también se han mostrado relacionados con la participación. Para mejorar la efectividad y disminuir las barreras a la participación, se recomiendan los cribados poblacionales organizados9.
El País Vasco muestra unas tasas ajustadas (población estándar europea) de incidencia (57,3/100.000; intervalo de confianza del 95% [IC95%]: 54,5-60 en 2008) y mortalidad (20,6/100.000; IC95%: 19,0-22,1 en 2009) relevantes, con incrementos significativos en ambas tasas, fundamentalmente en los hombres desde 1986-2008.12
El cribado poblacional, como estrategia para disminuir la incidencia y la mortalidad por cáncer colorrectal, fue aprobado en mayo de 2008 con los siguientes criterios: población diana entre 50 y 69 años de edad, cribado con SOH inmunoquímica cuantitativa cada 2 años y colonoscopia completa con sedación para confirmación de los casos positivos. Los requisitos para su implementación fueron: 1) sistema de información integrado con datos de pacientes; 2) coordinación del programa; y 3) coordinación de recursos públicos de atención primaria y atención especializada.
El objetivo de este trabajo es describir la estrategia del programa y los resultados en cuanto a participación y positividad de la prueba de SOH en la primera invitación en los años 2009-2011.
MétodoSe consideran elementos clave del programa la facilitación del acceso y la coordinación entre profesionales.
Organización del programaPuesta en marcha de un centro coordinador con un equipo técnico para su planificación, organización y evaluación. El acceso a las personas y profesionales se facilita por una línea telefónica gratuita y una cuenta de correo electrónico. Se desarrolló un aplicativo informático específico con identificación de todos los casos y se seleccionó la siguiente población: 1) pilotaje en 2009, 28.300 personas; 2) 116.980 personas de 31 unidades de atención primaria en 2010; y 3) 121.907 personas de 44 unidades en 2011. Se utilizó la base de datos de pacientes/usuarios del sistema público (95%-98% población residente de 50-69 años de edad). Se impartieron dos sesiones formativas previas a las invitaciones por parte de las unidades de atención primaria dirigidas a todo el personal de éstas.
Población invitableEn el centro coordinador se excluyeron las personas con antecedentes de cáncer colorrectal (Conjunto Mínimo Básico de Datos y Registro de Tumores) y con colonoscopia informada en los últimos 5 años.
Prueba de cribadoLas pruebas de SOH disponibles eran OC-Sensor® y Sentinel®, con un punto de corte de 100 ng/ml. Desde el 1 de junio de 2010 se utilizó OC-Sensor®.
Procedimiento de invitaciónTodas las cartas se enviaron desde el centro coordinador. La primera era de presentación, firmada por las autoridades sanitarias, con folleto informativo. En 8 a 10 semanas se envió la segunda carta, de invitación, que incluía el kit para realizar la prueba (recogida de heces), las instrucciones y el código identificador personal autoadhesivo utilizado para identificar y procesar la muestra. En la carta se informaba de que los resultados de participación serían conocidos por el médico de atención primaria. Se consideró como invitación válida toda carta no devuelta por correo.
ParticipaciónLas personas invitadas depositaron la prueba (kit) en un contenedor dispuesto en su centro de salud en horario abierto, sin trámites. En el centro se realizó la lectura óptica de la etiqueta identificativa de la muestra (fecha de participación), generando una petición vinculada al médico de primaria. Desde 2010 se envió carta de recuerdo.
Gestión de los resultadosTodas las muestras se procesaron en los laboratorios públicos de referencia de cada unidad de atención primaria, y los resultados fueron visibles en la historia clínica. El centro coordinador emite cartas personalizadas según los resultados: negativo, positivo y error. En caso positivo se indica al participante la necesidad de ser valorado por su médico, que le indicará una colonoscopia.
Análisis de los datosLas variables consideradas fueron: profesionales formados, edad en el momento de la invitación, sexo, fecha de recepción de la muestra, y fecha y resultado de la prueba de SOH. Los datos se extrajeron y analizaron con fecha del 31 de mayo de 2012, con SPSS v 20.0 y WINPEPI v 11.24. Se utilizó la prueba de ji al cuadrado para comparar porcentajes (con una significación estadística del 5%).
ResultadosSe impartieron 132 sesiones formativas, con un promedio de asistencia de las tres cuartas partes del personal objetivo de la formación, y con la participación de 75 unidades de primaria. No se encontraron diferencias significativas en cuanto a participación entre centros y profesionales.
De las 255.227 personas inicialmente seleccionadas como población diana en 2009-2011 (cobertura poblacional del 56,6%) se excluyeron 19.856 según los criterios de exclusión. El 2,3% de las exclusiones lo fueron por dirección desconocida. Se obtuvieron 235.371 invitaciones válidas.
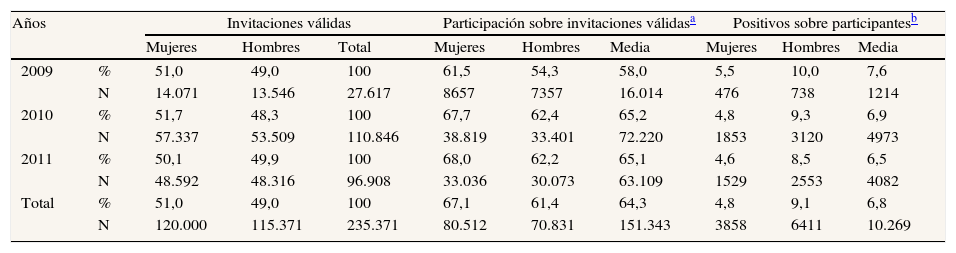
En la tabla 1 se presentan los principales resultados de 2009-2011. Se analizaron 151.176 muestras con resultado válido (positivo/negativo). La tasa de participación media fue del 64,3% (IC95%: 64,1-64,5) y la de positividad del 6,8% (IC95%: 6,7-6-9).
Invitaciones, participación y tasa de positividad de la prueba de sangre oculta en heces por año y sexo
| Años | Invitaciones válidas | Participación sobre invitaciones válidasa | Positivos sobre participantesb | |||||||
| Mujeres | Hombres | Total | Mujeres | Hombres | Media | Mujeres | Hombres | Media | ||
| 2009 | % | 51,0 | 49,0 | 100 | 61,5 | 54,3 | 58,0 | 5,5 | 10,0 | 7,6 |
| N | 14.071 | 13.546 | 27.617 | 8657 | 7357 | 16.014 | 476 | 738 | 1214 | |
| 2010 | % | 51,7 | 48,3 | 100 | 67,7 | 62,4 | 65,2 | 4,8 | 9,3 | 6,9 |
| N | 57.337 | 53.509 | 110.846 | 38.819 | 33.401 | 72.220 | 1853 | 3120 | 4973 | |
| 2011 | % | 50,1 | 49,9 | 100 | 68,0 | 62,2 | 65,1 | 4,6 | 8,5 | 6,5 |
| N | 48.592 | 48.316 | 96.908 | 33.036 | 30.073 | 63.109 | 1529 | 2553 | 4082 | |
| Total | % | 51,0 | 49,0 | 100 | 67,1 | 61,4 | 64,3 | 4,8 | 9,1 | 6,8 |
| N | 120.000 | 115.371 | 235.371 | 80.512 | 70.831 | 151.343 | 3858 | 6411 | 10.269 | |
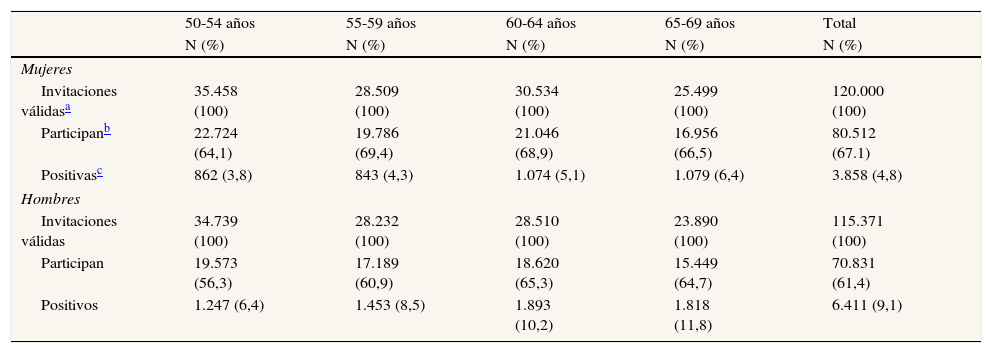
La participación de las mujeres fue significativamente superior a la de los hombres (p<0,001), con una media del 67,1% (IC95%: 66,9-67,4) frente al 61,4% de los hombres (IC95%: 61,1-61,7%). La tasa de positividad de la prueba de SOH entre las personas participantes fue significativamente superior en los hombres (p<0,001), con una media del 9,1% (IC95%:8,9-9,2) frente al 4,8% en las mujeres (IC95%: 4,7-4,9) (tabla 2).
Porcentajes de participación sobre población invitada y positividad de la prueba de sangre oculta en heces por grupo de edad y sexo
| 50-54 años | 55-59 años | 60-64 años | 65-69 años | Total | ||||||
| N (%) | N (%) | N (%) | N (%) | N (%) | ||||||
| Mujeres | ||||||||||
| Invitaciones válidasa | 35.458 (100) | 28.509 (100) | 30.534 (100) | 25.499 (100) | 120.000 (100) | |||||
| Participanb | 22.724 (64,1) | 19.786 (69,4) | 21.046 (68,9) | 16.956 (66,5) | 80.512 (67.1) | |||||
| Positivasc | 862 (3,8) | 843 (4,3) | 1.074 (5,1) | 1.079 (6,4) | 3.858 (4,8) | |||||
| Hombres | ||||||||||
| Invitaciones válidas | 34.739 (100) | 28.232 (100) | 28.510 (100) | 23.890 (100) | 115.371 (100) | |||||
| Participan | 19.573 (56,3) | 17.189 (60,9) | 18.620 (65,3) | 15.449 (64,7) | 70.831 (61,4) | |||||
| Positivos | 1.247 (6,4) | 1.453 (8,5) | 1.893 (10,2) | 1.818 (11,8) | 6.411 (9,1) | |||||
La tasa media de participación fue mayor que en los estudios comparados de cribados poblacionales, que la sitúan en el 42%.13 Estas superiores tasas también se encuentran en el cribado del cáncer de mama en el País Vasco respecto a la media estatal,14 lo que apunta a que pudieran estar involucrados factores sociales, culturales o de confianza en el sistema sanitario.
Las sesiones formativas y la implicación de los profesionales de atención primaria en el proceso pueden haber influido en estos resultados de participación que superan a los publicados y recomendados9.
La mayor participación de las mujeres podría asociarse a factores sociales y culturales,15 aunque habría que incorporar variables de deprivación, ruralidad o conocimientos previos, y hacerlo por áreas pequeñas.
El 50% de la participación se supera en ambos sexos y grupos de edad, lo cual hipotéticamente hace que esta intervención sea coste-efectiva, aunque para valorar su impacto se requieren estudios a medio plazo y relacionarlos con las lesiones detectadas.
La estrategia del programa parece disminuir las barreras de participación, al establecer facilidades para personas y profesionales. Deben estudiarse las diferencias con otros programas poblaciones para mejorar las estrategias organizativas.
Conseguir una participación superior al 50% es un reto de todos los programas de cribado. Se han publicado diversas estrategias organizativas para mejorarla, como la implicación de los médicos de atención primaria, remitir cartas personalizadas o enviar kits a domicilio.
¿Qué añade el estudio realizado a la literatura?La estrategia de implicación de atención primaria y facilitar la participación disminuyendo los trámites burocráticos podrían relacionarse con una alta participación.
Los autores firmantes han contribuido, desde su especialidad y servicio, a la puesta en marcha y la evaluación del programa en el País Vasco. Se considera necesaria la inclusión de más de seis autores dada la complejidad y la extensión del estudio realizado. Además, la Unidad de Epidemiología del Hospital Universitario de Cruces ha desarrollado herramientas de control de calidad de los datos y prestado soporte metodológico al programa. Todos los autores han realizado contribuciones previas al envío de este artículo.
FinanciaciónPara llevar a cabo este estudio se contó con una beca del Gobierno Vasco en el programa de ayudas a la investigación 2010. Expediente 2009111005.
Conflicto de interesesNinguno.
A las autoridades sanitarias de Osakidetza por la posibilidad de realizar este estudio y favorecer la formación y la implicación de todas las personas, especialmente de atención primaria, sin las que este programa no hubiese alcanzado tal éxito de participación. Especialmente a los referentes de las Comarcas de Atención Primaria: José Luis Hurtado, Eguskiñe Gallastegi, Carlos Antonio Pérez Pérez, María Luz Jauregi y Elisabeth Barandiaran, que han facilitado en sus centros y comarcas la buena marcha del programa. A epidemiólogos, endoscopistas, bioquímicos, enfermeras, patólogos, cirujanos, oncólogos, personal de citación y directivos, porque han hecho posible el diagnóstico precoz y el tratamiento de todas las personas. Un agradecimiento especial a Haritz Cortés por su dedicación y difusión del conocimiento, y al grupo de trabajo que impulsó este programa desde 2007 por su guía y su apoyo continuado a lo largo de este tiempo. Pero sobre todo, agradecemos la confianza depositada por la población en los profesionales y en el programa.